完善干细胞治疗临床技术指导,推动人体干细胞技术开发与应用

干细胞治疗作为再生医学的重要分支,在疾病治疗和组织修复领域展现出巨大潜力。随着又一版干细胞治疗征求意见稿的发布,我国临床试验技术指导体系正日趋完善,为人体干细胞技术的开发与应用注入了新的动力。
征求意见稿的不断更新反映了监管机构对干细胞治疗安全性与有效性的高度重视。通过明确细胞来源、质量控制、临床前研究和临床试验设计等关键环节,这些指导文件不仅为科研机构和医疗机构提供了操作规范,也保障了患者的权益。例如,新规要求干细胞产品必须经过严格的质量检测,确保无病原体污染和遗传稳定性,同时强调临床试验需遵循伦理审查和知情同同意原则。
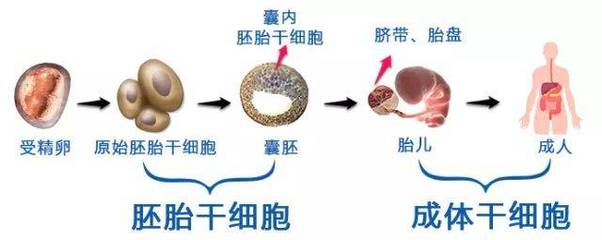
技术指导的完善推动了人体干细胞技术的创新开发。在基础研究层面,科研人员聚焦于诱导多能干细胞(iPSCs)、间充质干细胞(MSCs)等前沿方向,探索其在神经退行性疾病、心血管疾病和组织工程中的应用。监管框架的清晰化促进了产学研合作,加速了从实验室到临床的转化进程。企业可以依据指导文件优化产品管线,降低研发风险,从而提高技术落地效率。
临床试验的规范化是确保干细胞治疗安全有效的关键。征求意见稿细化了试验设计、终点指标和长期随访要求,帮助研究者设计更具科学性的方案。例如,在治疗罕见病或慢性疾病时,指导原则强调多中心、随机对照试验的重要性,以积累可靠证据。这不仅提升了我国干细胞研究的国际竞争力,也为全球干细胞治疗标准提供了参考。
随着技术指导的持续优化和行业实践的积累,人体干细胞技术有望在个性化医疗和再生医学中发挥更大作用。监管机构、科研界和产业界需加强协作,共同应对细胞异质性、长期安全性和规模化生产等挑战。通过不断完善政策框架,中国将加速干细胞治疗的产业化进程,造福更多患者。
如若转载,请注明出处:http://www.fadien.com/product/23.html
更新时间:2025-11-29 12:15:03